- লেখক Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:33.
- সর্বশেষ পরিবর্তিত 2025-06-01 07:36.
হাইড্রাজিন এবং কার্বোহাইড্রাইজাইডের মধ্যে মূল পার্থক্য হল যে হাইড্রাজিনে H2N-NH2 গঠন থাকে যেখানে কার্বোহাইড্রাইজাইডে দুটি হাইড্রাজিন অণু থাকে যা একটি একক কার্বনাইল কার্বন কেন্দ্রের সাথে সংযুক্ত থাকে।
হাইড্রাজিন এবং কার্বোহাইড্রাইজাইড হল রাসায়নিক যৌগ যার মধ্যে H2N-NH2 একক রয়েছে। এই রাসায়নিক কাঠামোর একটি একককে হাইড্রাজিন বলা হয় যখন কার্বোহাইড্রাইজাইডের মধ্যে এই দুটি কাঠামো একটি কার্বনাইল কার্বন কেন্দ্রের সাথে সংযুক্ত থাকে।
Hydrazine কি?
Hydrazine রাসায়নিক সূত্র N2H4 সহ একটি অজৈব যৌগ। আমরা এটিকে একটি সাধারণ পিনিটোজেন হাইড্রাইড হিসাবে নাম দিতে পারি এবং এটি একটি বর্ণহীন এবং দাহ্য তরল যার একটি অ্যামোনিকাল গন্ধ রয়েছে।এই যৌগটি অত্যন্ত বিষাক্ত, এবং আমাদের এই পদার্থটিকে যত্ন সহকারে পরিচালনা করা উচিত। এটির বিষাক্ততা হ্রাস পায় যদি এটি একটি দ্রবণে ব্যবহার করা হয়, যেমন হাইড্রাজিন হাইড্রেট।

চিত্র 01: হাইড্রাজিন হাইড্রেট
Hydrazine প্রধানত একটি ফোমিং এজেন্ট হিসাবে উপযোগী, যা পলিমার ফোম তৈরিতে গুরুত্বপূর্ণ। অধিকন্তু, এটি পলিমারাইজেশন অনুঘটক, ফার্মাসিউটিক্যালস এবং এগ্রোকেমিক্যালের অগ্রদূত হিসেবে উপযোগী, সেইসাথে মহাকাশে মহাকাশযান চালনার জন্য দীর্ঘমেয়াদী সংরক্ষণযোগ্য প্রপেলান্ট।
হাইড্রাজিন উৎপাদনের জন্য অনেকগুলি ভিন্ন রুট রয়েছে, যার মধ্যে পারঅক্সাইড থেকে অক্সাজিরিডাইনের মাধ্যমে অ্যামোনিয়ার জারণ, ক্লোরিন-ভিত্তিক অক্সিডেশন ইত্যাদি। হাইড্রাজিনের প্রতিক্রিয়া বিবেচনা করার সময়, এটি অ্যাসিড-বেস আচরণ দেখায় যেখানে হাইড্রাজিন একটি গঠন করতে পারে। মনোহাইড্রেট যা অ্যানহাইড্রাস ফর্মের চেয়ে ঘন, এবং এতে মৌলিক (ক্ষার) বৈশিষ্ট্য রয়েছে যা অ্যামোনিয়ার সাথে তুলনীয়।উপরন্তু, হাইড্রাজিন রেডক্স প্রতিক্রিয়ার মধ্য দিয়ে যেতে পারে কারণ এটি একটি হ্রাসকারী হিসাবে কাজ করতে পারে, যা সাধারণত নাইট্রোজেন এবং জলের উপজাত প্রদান করে৷
কার্বোহাইড্রাইজাইড কি?
Carbohydrazide হল একটি জৈব যৌগ যার রাসায়নিক সূত্র H4N2-C(=O)-N2H4 রয়েছে। এই পদার্থটি একটি সাদা, জলে দ্রবণীয় কঠিন হিসাবে উপস্থিত হয় যা গলে যাওয়ার পরে পচে যায়। এমন অনেকগুলি কার্বাজাইড রয়েছে যেগুলির এক বা একাধিক N-H গ্রুপ অন্যান্য বিকল্প দ্বারা প্রতিস্থাপিত হয়েছে৷
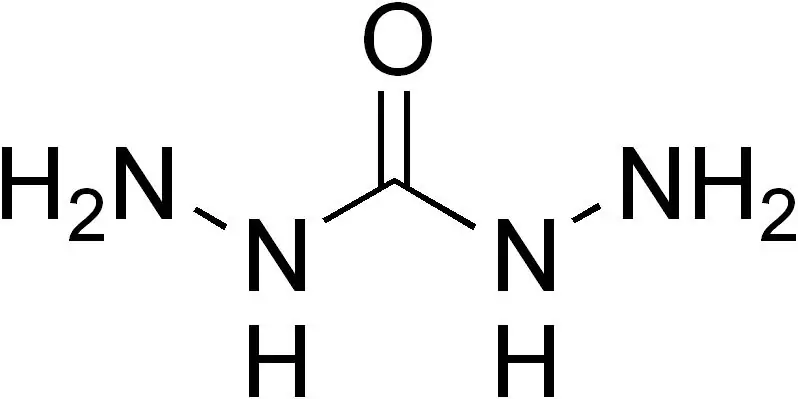
চিত্র 02: কার্বোহাইড্রাইজাইড অণুর গঠন
আমরা হাইড্রাজিন দিয়ে ইউরিয়া চিকিত্সার মাধ্যমে শিল্পভাবে এই পদার্থটি তৈরি করতে পারি। এছাড়াও, আমরা কার্বনেট এস্টার সহ হাইড্রাজিনের সাথে অন্যান্য C1 অগ্রদূতের প্রতিক্রিয়ার মাধ্যমে এই পদার্থটি প্রস্তুত করতে পারি।
কার্বোহাইড্রাইজাইড অণু একটি অ-পোলার অণু, এবং এই অণুর সমস্ত নাইট্রোজেন কেন্দ্র অন্তত কিছুটা পিরামিডাল, যা একটি দুর্বল C-N পাই বন্ধন নির্দেশ করে৷
এই যৌগটির ব্যবহার বিবেচনা করার সময়, এটি একটি অক্সিজেন স্ক্রাবার, পলিমারের অগ্রদূত, স্টেবিলাইজার হিসাবে ফটোগ্রাফিতে দরকারী, গোলাবারুদ প্রোপেল্যান্ট, স্থিতিশীল সাবান ইত্যাদির বিকাশে গুরুত্বপূর্ণ।
Hydrazine এবং Carbohydrazide এর মধ্যে পার্থক্য কি?
Hydrazine এবং carbohydrazide হল নাইট্রোজেনযুক্ত রাসায়নিক যৌগ। হাইড্রাজিন এবং কার্বোহাইড্রাইজাইডের মধ্যে মূল পার্থক্য হল যে হাইড্রাজিনে H2N-NH2 গঠন থাকে যেখানে কার্বোহাইড্রাইজাইডে দুটি হাইড্রাজিন অণু থাকে যা একটি একক কার্বনাইল কার্বন কেন্দ্রের সাথে সংযুক্ত থাকে। তদুপরি, আমরা হাইড্রাজিনকে একটি অজৈব যৌগ এবং কার্বোহাইড্রাইজাইডকে একটি জৈব যৌগ হিসাবে শ্রেণীবদ্ধ করতে পারি কারণ হাইড্রাজিনের অণুতে কার্বন পরমাণু নেই যদিও কার্বোহাইড্রাইজাইডে একটি কার্বনাইল কার্বন কেন্দ্র রয়েছে৷
এছাড়া, আমরা পারঅক্সাইড, ক্লোরিন-ভিত্তিক অক্সিডেশন ইত্যাদি থেকে অক্সাজিরিডাইনের মাধ্যমে অ্যামোনিয়ার অক্সিডেশন এবং হাইড্রাজিন দিয়ে ইউরিয়া চিকিত্সার মাধ্যমে কার্বোহাইড্রাইজাইড ব্যবহার করে হাইড্রাজিন তৈরি করতে পারি।
নিচের ইনফোগ্রাফিক সারণী আকারে হাইড্রাজিন এবং কার্বোহাইড্রাইজাইডের মধ্যে পার্থক্যের আরও বিশদ বিবরণ দেখায়৷

সারাংশ - হাইড্রাজিন বনাম কার্বোহাইড্রাইজাইড
Hydrazine এবং carbohydrazide হল নাইট্রোজেনযুক্ত রাসায়নিক যৌগ। হাইড্রাজিন এবং কার্বোহাইড্রাইজাইডের মধ্যে মূল পার্থক্য হল যে হাইড্রাজিনে H2N-NH2 গঠন থাকে যেখানে কার্বোহাইড্রাইজাইডে দুটি হাইড্রাজিন অণু থাকে যা একটি একক কার্বনাইল কার্বন কেন্দ্রের সাথে সংযুক্ত থাকে। তাছাড়া, হাইড্রাজিন একটি বর্ণহীন তরল হিসাবে ঘটে যখন কার্বোহাইড্রাইজাইড একটি সাদা রঙের কঠিন পদার্থ হিসাবে ঘটে।






